�ֽ��ǽ����Ŷ���ֲ��Ĥ����̬���㷽�淢����������������
���գ�������ҵ��ѧ��ľ����������ָ߾��ⴴ�����ĺ�����ѧԺ�ֽ��ǽ���������ֲ��ѧȨ��ѧ���ڿ�Annual Review of Plant Biologyд��Ϊ ��Exploring the Spatiotemporal Organization of Membrane Proteins in Living Plant Cells������������ (IF=22.8)�����ڻ���״̬��ֲ��Ĥ����̬���ۺ�״̬���������ĵ����ӷ��������������ܽᣬ����Щ�����ӷ���������ֲ������ѧ�е�Ӧ�ý���������̽�֣����������Ч�ķ���������
ֲ��Ĥ����������ת�˺��ź�ת�������з�����Ҫ���ã����ڻ����������о��ͷ���Ĥ���Ķ�̬���̡����Ӽ��������dz����ѡ��ֽ��ǽ����о��Ŷ����Ƚ������ʺ���ֲ���ϸ���۲�ĵ����ӷ���ƽ̨��ʵ�������塢ԭλ������Ĥ���ۺ�״̬�Լ������������ͺ��뼶��ʵʱ��̬��⡣ʮ��������ͨ�������Ӽ�����̶�ֲ���е�PIP2;1 (Li et al., Plant Cell, 2011), Flot1 (Li et al., Plant Cell, 2012), AMT1;3 (Wang et al., PNAS, 2013), AP2 �� (Fan et al., Development, 2013), Phot1 (Wan et al., Plant Cell, 2014), RbohD (Hao et al., Plant Cell, 2014), BRI1 (Wang et al., Molecular Plant, 2015) ��Ĥ������ɢ��פ��ʱ��ȶ�̬���������˼��ͷ���������, ��ͨ���Ż������Ӽ����������˻���״̬��Ĥ���ľۺ�״̬ (Wang et al., Nature Protocols, 2015)����������һЩ��Ҫϸ����Ĥ���ĵ����Ӽ�⼼������ (Lv et al., Molecular Plant, 2017)���ڹ�ȥ��Щ�о��Ļ����ϣ����������ط��IJ���������ֲ��Ĥ���������о�������������Ǽ����������ӳ�������Ĥ���ۺ���ͻ����Ķ�̬���㷽�����Լ���Щ������ֲ������ѧ�����Ӧ�á�
���ڵ������ӵ�ӫ����������������ܵ����������ĸ��ţ����Ҫʵ�ֵ����ӳ���Ĥ��������Ч���������Ҫ���������ĵ�һ���ֳ��˽��ܳ���ı�Ƿ�����Ʃ��С����Ⱦ�Ϻ�����ӫ��������(���ӵ�QD)�ȼ����⣬���ص�������ӫ�⵰�ı��(��GFP��mCherry��DsRed-E5���⼤���PA-GFP��Dronpa)���Լ�������ʵ��Ӧ������Ҫע������⡣
�ڶ����ֲ����˱�Ǻĵ������ٺͳ���������������۽����������߷ֱ������Ϳ��������ȡ���Ȼ����Ĺ��۽������ķֱ��ʲ��ܴﵽ�����Ӽ��Ҫ��������ø������ȵļ�����������Ӧ�ķ���ϵͳ��Ʃ��ӫ����ع���(FCS)��ӫ�⻥��ع���(FCCS)��ӫ����������ƫ��(FRET)�����ȣ�Ҳ����ʵ�ֶԵ����ӵ��١���̬�����Լ�Ĥ����״̬�ļ�⡣���������˽���2014��ŵ������ѧ������ij��ֱ�����(STED��STORM��PALM��)���⣬�ص�������ʺ���ֲ��ϸ��Ĥ�������Ŀɱ�Ƕ�-ȫ�ڷ���ӫ������(VA-TIRFM)��ԭ������Ӧ�á�
�����ĵ���������ϸ�������ڱ�Ǻͳ�������ϣ��ⶨĤ���ۺ�״̬�Ͷ���ѧ��������Ҫ������(1)ͨ��ӫ��ǿ�ȵķ�������������FIDA��PCH��SpIDA������(2)ͨ��ӫ��Ư�ķ�������������smSubunit-counting��smFRAP������(3)ͨ��ӫ�����估ӫ�������ת�Ƶķ�������������FCS/FCCS��FRET-FLIM������(4)ͨ��������λ������õķ�������������������ˮƽ�ĵ��ӽ�ָ����������(smPPI)�͵�����ˮƽ��pull-down ������
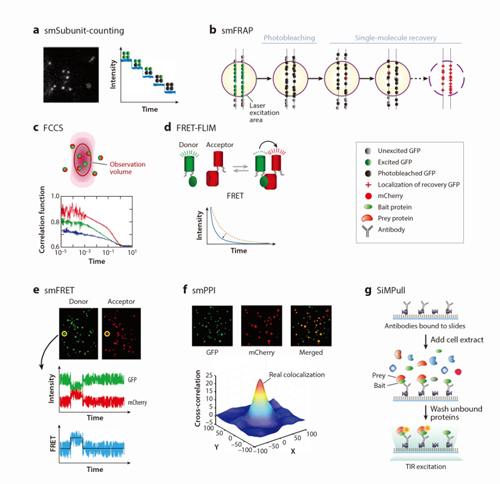
ͼ1ֲ��ϸ����Ĥ���ۺ�״̬�Ķ�̬���㼼��ģʽͼ
���������һ���ּ�Ҫ���������źŴ��������У������Ӽ������ڼ��Ĥ���ۺ���״̬����̬�仯��Ĥ����ϵ������ѧ������ϸ���Ǽܹ�ϵ���Լ���ͬ����������Ĥ�����ܶȡ�פ��ʱ�䡢����;����ת�����ʡ�ϸ���Ǽܺ�ϸ���ڶ�Ĥ���ۺ����γɵĶ�̬���صȷ����Ӧ�ã�Ϊֲ��Ĥ�����о��ṩ����˼·��
����������4��6�����߷���(https://doi.org/10.1146/annurev-arplant-042817-040233)���ֽ��ǽ���Ϊ���ĵ�ͨѶ���ߣ����Ŷӳ�Ա����Ϊ���ݴ�ѧ����������Ϊ���ĵĵ�һ���ߣ��Ŷӳ�ԱѦ��Ⱥ���Ͼ������ο���ʿΪ���ĵ��������ߡ������ĵõ��˱�����ľ����������ָ߾��ⴴ�����ĺ�����Ȼ��ѧ�����ص���Ŀ��������


